Paolo Maccallini, 29 augustus 2017
Laatste nieuws
 Tijdens het gemeenschapsymposium over de moleculaire basis van ME/cvs (R) rapporteerden twee verschillende onderzoeksgroepen een toegenomen niveau van antistoffen tegen bèta-adrenerge en muscarinereceptoren in sera van ME/cvs-patiënten versus gezonde controles (Figuur 1.) Deze nieuwe data zijn onafhankelijk verzameld door Alan Light (University of Utah) en Jonas Bergquist (Uppsala Universitet). Bergquist gaf ook aan dat deze autoantilichamen niet kunnen worden gevonden in de cerebrospinale vloeistof van ME/cvs-patiënten.
Tijdens het gemeenschapsymposium over de moleculaire basis van ME/cvs (R) rapporteerden twee verschillende onderzoeksgroepen een toegenomen niveau van antistoffen tegen bèta-adrenerge en muscarinereceptoren in sera van ME/cvs-patiënten versus gezonde controles (Figuur 1.) Deze nieuwe data zijn onafhankelijk verzameld door Alan Light (University of Utah) en Jonas Bergquist (Uppsala Universitet). Bergquist gaf ook aan dat deze autoantilichamen niet kunnen worden gevonden in de cerebrospinale vloeistof van ME/cvs-patiënten.
Voorlopige resultaten
|
Resultaten van onze Pilotstudie over Auto-immuniteit in ME/CVS
|
Figuur 1. Twee dia’s van het symposium: links data van Uppsala Universitet, rechts data van een groep van patiënten bestudeerd door Alan Light (University of Utah).
Wat al bekend was over deze autoantilichamen
De aanwezigheid van een hoger dan normale reactiviteit van sera van ME/cvs-patiënten tegen muscarinereceptoren werd voor het eerst meer dan een decennium geleden gemeld door een Japanse groep (Tanaka S et al. 2003) en is onlangs bevestigd in een werk van de Universiteit van Bergen (Noorwegen) en de Charité-Universiteit (Duitsland) (Loebel M et al. 2016). In het bijzonder, terwijl Tanaka en collega’s een verhoogd niveau van autoantilichamen tegen cholinerge muscarinereceptor 1 (CHRM1) maten in ongeveer de helft van de patiënten, beschreef de andere groep een verhoging in reactiviteit van sera op subtypen M3 en M4, in een subgroep van patiënten (figuur 2). Ze gebruikten twee volledig verschillende testen, zoals we later zullen zien, en dit zou de reden voor de verschillende resultaten kunnen zijn.
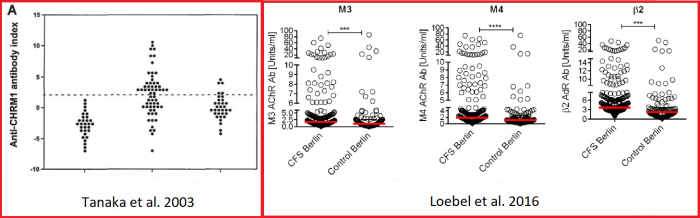
Figuur 2. Een toename van reactiviteit van sera van ME/cvs-patiënten op M1 cholinerge receptoren door Tanaka en collega’s in 2003 (links). Loebel en collega’s vonden een toename in reactiviteit op M3 M4 cholinerge receptoren en bèta-2 adrenerge receptoren in 2016 (rechts).
Zoals je kunt zien in figuur 2, laat de studie van Loebel et al. ook een toename in antilichamen tegen bèta-adrenerge receptoren (subtype 2) zien, in overeenkomst met de laatste data van Light en Bergquist. In dit verband moet worden opgemerkt dat autoantilichamen tegen muscarinereceptoren M2 en M3 en tegen bèta adrenerge receptoren (subtype 1 en 2) reeds zijn waargenomen in orthostatische hypotensie (OH) (Yu X et al. 2012), (Li H et al. 2012) en dat antilichamen tegen bèta-2 adrenerge receptoren zijn vastgesteld bij patiënten met Posturaal Orthostatisch Tachycardiesyndroom (POTS) (Li et al. 2014). Dit betekent dat deze groep auto-antilichamen in verband wordt gebracht met orthostatische intolerantie (POTS en/of OH), maar orthostatische intolerantie is ook een onderdeel van het klinische beeld van ME/cvs (IOM 2015) en de patiënten die zijn gediagnosticeerd met POTS, hebben vaak veel kenmerken gemeen met ME/cvs-patiënten, zie bijvoorbeeld (Okamoto L et al. 2012), (Wise S et al. 2015). Het is dus denkbaar dat deze autoantilichamen een rol spelen in de pathogenese van enkele symptomen van een subgroep van patiënten, hoewel dit tot nu toe niet bewezen is.
Moleculaire nabootsing?
We weten niet waarom het immuunsysteem van sommige ME/cvs-patiënten reageert op deze receptoren, maar Alan Light gaf tijdens het symposium aan dat een mogelijke oorzaak voor deze antilichamen wellicht een mechanisme is dat moleculaire nabootsing [moleculaire mimicry] wordt genoemd. De basisidee achter moleculaire nabootsing is dat B-cellen per vergissing antilichamen produceren tegen menselijke proteïnen wanneer epitopen van een infectie erg lijken op de epitopen die gevonden worden in de gastheer (Rose NR 1998). Van moleculaire nabootsing wordt op dit moment geloofd dat het de pathogenese van het Guillain-Barré-Syndroom verklaart, waarbij de lipo-oligosacchariden op het buitenmembraan van campylobacter jejuni een immuunreactie op menselijke gangliosiden lijkt te ontlokken (in vatbare individuen), als gevolg van de gelijkenis tussen deze antigenen (Van den Berg B et al. 2014). Welnu, als moleculaire nabootsing betrokken is bij de oorsprong van de antilichamen tegen bèta-2 adrenerge receptoren, welke is dan de epitoop van de receptor? En welke het door een pathogeen overgedragen antigeen? Om een mogelijk antwoord op deze vraag te vinden moeten we in acht nemen dat de gebieden van de receptoren die betrokken kunnen zijn in B-cel auto-immuniteit alleen die kunnen zijn die een extracellulaire blootstelling hebben; de andere gebieden zijn ondergedompeld in plasmamembraan en in cytoplasma en kunnen zodoende niet met antilichamen communiceren. Zoals te zien is in Figuur 3, heeft bèta-2 adrenerge receptor (ADRB2) vier extracellulaire gebieden, voornamelijk peptides 1-34, 96-106, 175-196, 299-305. In het algemeen zijn epitopen voornamelijk conformationeel wat betekent dat zij gebieden van het eiwitoppervlak zijn, veroorzaakt door het vouwen van de eiwitten. Niettemin zoeken we in ons voorbeeld alleen lineaire epitopen.
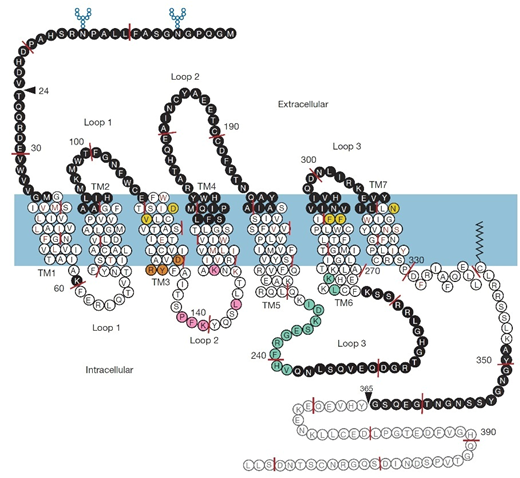
Figuur 3 . Schematische representatie van ADRB2, van (Rasmussen G et al. 2007). Je ziet de extracellulaire peptiden 1-34 (de N-terminus), 96-106 (lus 1), 175-196 (lus 2), 299-305 (lus 3).
Ik heb QuickBLASTP van NCBI gebruikt, voorzien van de standaardinstellingen (E = 100, een woord van 6 letters, BLOSUM62 als vervangingsmatrix) en ik heb voor elk van de vier extracellulaire peptiden zowel de sequentie van residuen van de N-terminus tot de C-terminus, als de omgekeerde sequentie overwogen. We krijgen als enige overeenkomst het eiwit sensor histidine kinase MtrB, dat behoort tot Pseudonocardia sp. Ae331_Ps2 (R) (figuur 4). Ik kan dit bepaalde eiwit in UniProt niet vinden, maar als het een membraaneiwit was en als peptide 67-77 werd blootgesteld aan extracellulaire ruimte, kan deze peptide misschien een kandidaat zijn als een trigger voor anti-ADRB2, volgens de moleculaire nabootsingstheorie. Het is belangrijk op te merken dat hoewel moleculaire nabootsing een populaire theorie is (misschien vanwege haar eenvoud) het alleen in het Guillain-Barré-syndroom een bewezen oorzaak is van auto-immuniteit.
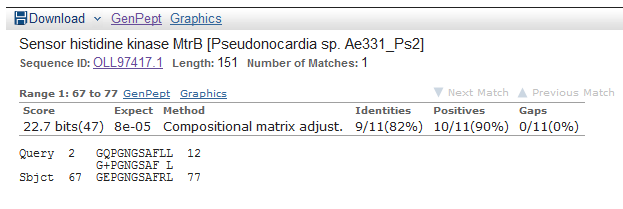
Figuur 4. Peptide 2-12 van de ADRB2-receptor lijkt op peptide 67-77 van sensor histidine kinase MtrB (van Pseudonocardia sp. Ae331_Ps2).
Dus, waarom geen test voor deze autoantilichamen?
Als antilichamen tegen adrenerge en muscarinereceptoren betrokken zijn bij de pathogenese in sommige gevallen van ME/cvs, zou het voor patiënten interessant zijn dit te testen. In dit verband wil ik erop wijzen dat het meten van antilichamen tegen membraanreceptoren moet worden gedaan met een test waarin deze receptoren worden uitgedrukt door levende cellen in hun fysiologisch omgeving (celgebaseerde test). In feite, met testen waarbij receptoren in een laagje op plaatjes worden aangebracht, krijgen we zowel vals positieve resultaten (als gevolg van het feit dat sera reageren op peptides die zich niet in het extracellular domein bevinden) als vals negatieve (als gevolg van eiwitdenaturatie, wat leidt tot de vorming van epitopen die niet aanwezig zouden zijn als de eiwitten correct gevouwen zouden zijn). De superioriteit van celgebaseerde testen tegenover de andere soort testen wordt algemeen aanvaard in het geval van anti-MOG-antilichamen (Ramanathan S et al 2016). Het dient te worden vermeld dat de studie door Loebel et al. een celgebaseerde test gebruikt, terwijl de vorige studie op plaatjes gecoate recombinante eiwitten gebruikte (Tanaka et al.). Dit kan de reden zijn voor de discrepantie tussen de resultaten van de twee studies (figuur 2). Voor zover ik weet, zijn er op dit moment geen commerciële celgebaseerde testen voor anti-muscarine-cholinerge receptoren en bèta-adrenerge receptoren. Uit de verstrekte documentatie lijkt de enige beschikbare test geen celgebaseerde test (R) te zijn.
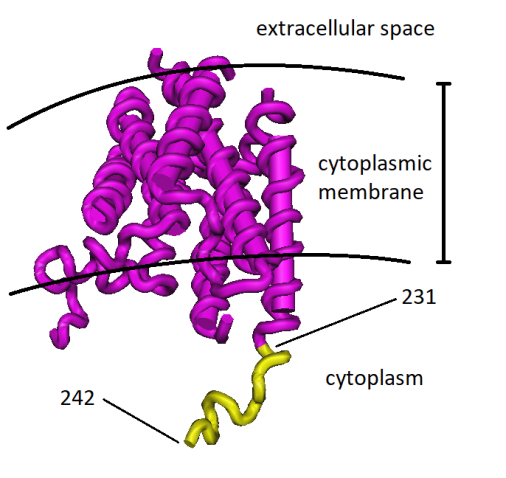
Figuur 5. In geel: de epitoop voorspeld door DiscoTope 2.0 op de 3D-structuur van ADRB2 (PDB-ID: 2R4R keten A). Ik heb ook aangegeven welk deel van het molecuul buiten de cel valt, wat er in het membraan zit en wat in de cel.
Experiment in silico
We zullen nu proberen te simuleren wat er zou gebeuren met een zoektest naar anti-ADB2R antilichamen, als het eiwit was gecoat op een plaatje. We zullen de voorspelling van DiscoTope 2.0 gebruiken, wat een software is die alle mogelijke B-cell-epitopen berekent van een bepaald eiwit, gebruikmakend van zowel de geometrie van het eiwit (met name een parameter genaamd uitsteekselindex, berekend uit de traagheidsellipsoïde van het eiwit) en statistische data over bekende B-cell-epitopen (Kringelum, et al., 2012). Wanneer we de 3D–structuur van ADB2R gebruiken die experimenteel is bepaald in (Rasmussen et al. 2007) met standaard instellingen, DiscoTope voorspelt peptide 231-242 als de enig mogelijke epitoop (bedenk dat de experimentele 3D-structuur van ADB2R niet compleet is). Zoals je kunt zien in figuur 5 behoort deze peptide tot het intracellulaire domein van de receptor en kan daarom in geen geval een B-cell-epitoop zijn, in vivo. Kortom, volgens deze simulatie bestaat het risico van vals positieve resultaten bij elke test die gebruik maakt van recombinant ADB2R gecoat op een plaatje.
© Paolo Maccallini. Vertaling tanto, redactie abby, ME-gids.





