Cort Johnson, Simmaron Research, 4 augustus 2018
 Epigenetisch onderzoek biedt de fascinerende mogelijkheid om uit te zoeken welke verschuiving er precies plaatsvond bij het ontstaan van ME/CVS. Voor veel ME/CVS-patiënten trad er een plotse verandering op, een soort van biologische reset die zich nooit helemaal herstelde.
Epigenetisch onderzoek biedt de fascinerende mogelijkheid om uit te zoeken welke verschuiving er precies plaatsvond bij het ontstaan van ME/CVS. Voor veel ME/CVS-patiënten trad er een plotse verandering op, een soort van biologische reset die zich nooit helemaal herstelde.
Uitzoeken welke ‘reset’ er precies heeft plaatsgevonden, is waar het bij epigenetica om draait. Epigenetica identificeert veranderingen in de expressie van onze genen die optreden nadat we in aanraking komen met biologische stressoren zoals ziekteverwekkers, geneesmiddelen, toxines of zelfs voedingsmiddelen.
De meeste van onze genen die pro-inflammatoire cytokinen produceren, hebben een soort slot in zich. Als dat slot verwijderd wordt, kunnen de genen zichzelf tot uitdrukking brengen en mogelijk onze gezondheid beschadigen.
Epigenetica onderzoekt hoe de biologische stressoren die we in het leven tegenkomen, deze sloten kunnen openbreken (of ze nog vaster te zetten) met als resultaat een geheel nieuw genetisch landschap – één dat misschien wel iets als ME/CVS kan veroorzaken.
Bij veel patiënten met ME/CVS of fibromyalgie begon hun ziekte met een infectie, en virussen kunnen belangrijke epigenetische veranderingen in ons genoom teweeg brengen. Het herpes-simplexvirus (het virus waar dokter Pridgen zich op richt in fibromyalgie) brengt bijvoorbeeld veranderingen aan in ons genoom die het virus helpen om vernietiging te voorkomen, en zijn replicatie te verbeteren. Die veranderingen omvatten onder meer een onderdrukking van ons immuunsysteem, wat kan resulteren in een verhoogd risico op kanker.
Maar boontje komt om zijn loontje. Epigenetic News berichtte onlangs dat een kankermedicijn dat zich op epigenetische wijzigingen richt, in staat was tot het herstellen van de delen van het immuunsysteem die ontregeld waren door het herpes-simplexvirus. Het medicijn was in staat om de tekorten in het immuunsysteem die het virus had veroorzaakt, op te vullen door het stimuleren van een aantal immuunfactoren (IFN-a, IL-8, IL-6, transcriptiefactoren, stressresponsfactoren). Studies op muizen lieten zien dat het medicijn ook de reactivatie van het virus vermindert.
Dat suggereert dat sommige gelijkaardige medicijnen die nu in klinische studies worden getest, zouden kunnen helpen in de bestrijding van herpes en andere virussen, of misschien gewoon weer normale epigenetisch gemodificeerde genen zouden kunnen worden die een onderdrukte immuunfunctie hebben.
“Een nieuwe soort antivirale middelen op basis van deze studie zou nuttig kunnen zijn voor patiënten die niet reageren op bestaande antivirale middelen zoals aciclovir en ganciclovir…. (of in) virale infecties waarvoor geen geneesmiddelen bestaan om de immuunrespons van de patiënt te stimuleren.” Dr Kristie.
Als epigenetica een even belangrijke rol blijkt te spelen in ME/CVS als in kanker en andere ziekten, dan kan een kankermedicijn misschien ooit gebruikt worden als ME/CVS-therapie.
Epigenetische studie benadrukt wijzigingen in het immuunsysteem in ME/CVS
Het epigenitcaverhaal begint met gentranscriptie – de eerste stap in het proces van het vertalen van onze genen in eiwitten. Genexpressie wordt mogelijk gemaakt door het verwijderen van methylgroepen die transcriptie blokkeren en/of door het toevoegen van methylgroepen die voorkomen dat genen tot expressie komen.
Malay Trivedi en Lubov Nathanson aan het Institute of Neuroimmune Research van dokter Nancy Klimas aan de Nova Southeastern University publiceerden onlangs de meest uitgebreide studie tot nog toe over epigenetica bij ME/CVS.
Er zijn slechts paar epigenetische studies uitgevoerd in ME/CVS, en geen enkele zoals deze. Zo profiteerde de onderzoeksgroep van een nieuwe doorbraak in genetische testmethodes (een geavanceerde array van Illumina) die toeliet bijna dubbel zo veel gebieden te testen (850.000 in plaats van 450.000) als voorheen. Verder maakte de grotere steekproef (met 64 proefpersonen afkomstig uit twee geografisch ver uit elkaar liggende locaties) het mogelijk om de epigenetische veranderingen in ME/CVS grondiger te bestuderen. Zo kon de onderzoeksgroep wijzen op wat de auteurs “overeenstemmende gehypomethyleerde gebieden” noemden, die volgens hen bij volgend onderzoek gebruikt kunnen worden.
De algemene bevindingen van deze studie stemden overeen met die van eerdere epigenetische studies bij ME/CVS. Hypomethylatie – het verwijderen van methylgroepen, wat het gemakkelijker maakt voor genen om tot uitdrukking te komen – kwam steeds opnieuw terug: in 98% van de ME/CVS-gebieden die in DNA-methylatie van gezonde controles verschilden, betrof het hypomethylatie (in slechts 2% ging het om hypermethylatie in vergelijking met controles). De hypomethylatie was vooral aanwezig in genen die betrokken zijn bij de regulatie van immuuncellen.
De hoge mate van hypomethylatie was om verschillende redenen intrigerend. Zo veroorzaakt het Epstein-Barr-virus – waarschijnlijk een veelvoorkomende oorzaak van ME/CVS – overwegend hypomethylatie en bijna nooit hypermethylatie van genen. Hypomethylatie wordt ook geassocieerd met pro-inflammatoire genexpressie in auto-immuunziekten alsook in de ontwikkeling van kanker.
Doorbraak in multiple sclerose
Een “globale” hypomethylatie, wordt bijvoorbeeld ook gevonden in lupus en reumatoïde artritis. De hypomethylatie van een promotorgen voor IL-6 veroorzaakt in reumatoïde artritis een overexpressie van pro-inflammatoire cytokines en andere immuunfactoren die uiteindelijk resulteren in gewrichtsschade.
De onlangs ontdekte hypomethylatie van een HLA-gen bij multiple sclerose (MS) heeft onderzoekers ertoe aangezet te beweren dat epigenetische veranderingen zelfs “oorzaak van de ziekte” kunnen zijn. Deze stoutmoedige verklaring weerspiegelt de bevindingen van een recente grote studie, die aangaf dat epigenetische veranderingen rechtstreeks verantwoordelijk zijn voor de belangrijkste risicofactor tot nu toe die voor MS gevonden werd.
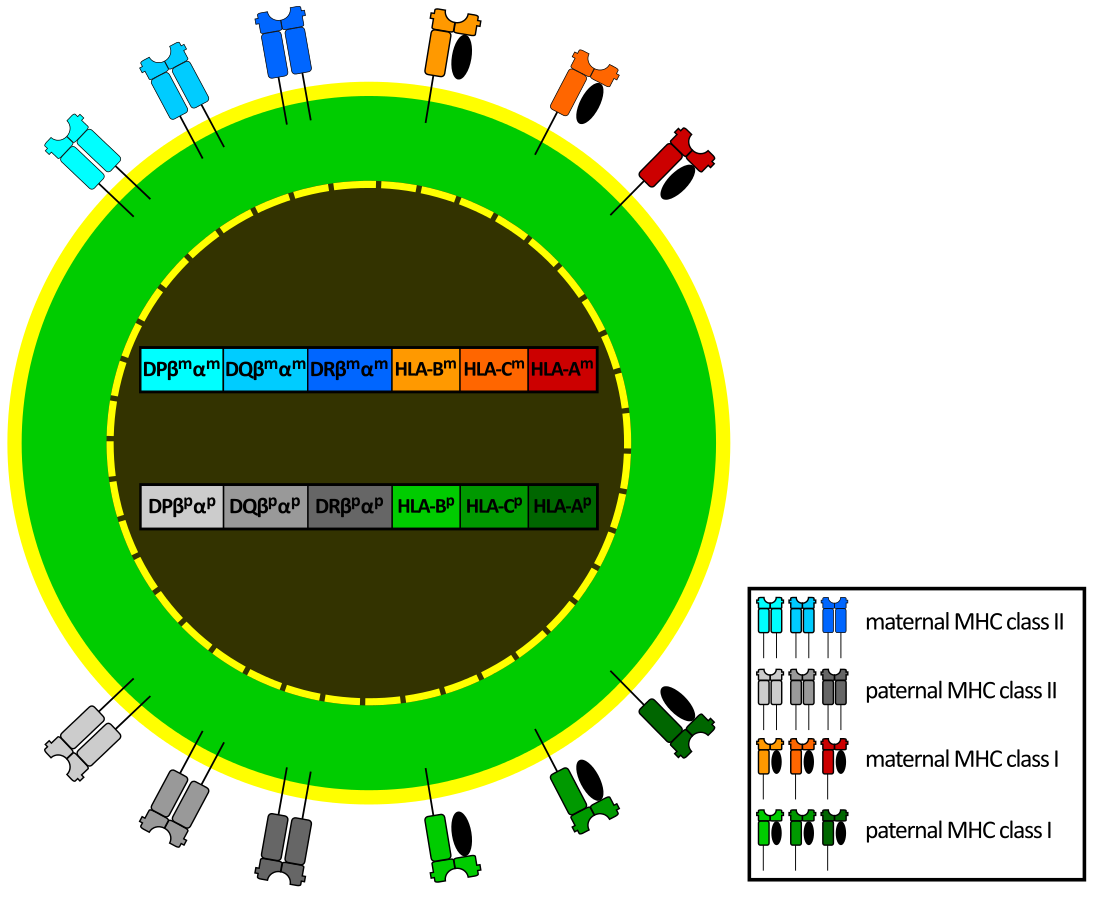
Epigenetische veranderingen aan de HLA-genen zouden MS in gang kunnen zetten. © ZionLion77 via Wikipedia
Deze bevinding kan gevolgen hebben die veel verder reiken dan MS, mogelijk zelfs tot bij ME/CVS en fibromyalgie. Aangezien de HLA-regio van het genoom geassocieerd wordt met bijna alle auto-immuunziekten, denken de auteurs van de studie dat hun resultaten een impact zullen hebben op andere auto-immuunziekten.
(Enkele jaren geleden wees Ron Davis de HLA-regio al aan als potentieel studiegebied voor ME/CVS. Zijn Stanford Genome Lab heeft nieuwe methoden ontwikkeld om deze complexe regio van ons genoom te onderzoeken, en hij en Mike Snyder uit Stanford maken een intensieve analyse van die HLA-regio in ME/CVS.)
Terug naar ME/CVS
De hoogste graad van hypomethylatie in ME/CVS vond men in een regio van het genoom die de werking van naturalkillercellen (NK-cellen) stimuleert (een verminderde NK-functie is een van de meest consistente bevindingen in ME/CVS). Dit suggereerde dat een soort van epigenetische reset – misschien getriggerd door een infectie – voorkwam in de NK-cellen van ME/CVS-patiënten.
Met betrekking tot enkelvoudige genen wijzen de auteurs op de hypomethylatie van genen die geassocieerd zijn met: spierhypotonie (lage spiertonus), cognitieve stoornissen (MED13L), problemen met eiwitsynthese (metabolisme) en glucocorticoïden (SGK-gen – ontsteking).
Het waren echter de immuungerelateerde genen waar de hypomethylatie het sterkst naar voren kwam. Immuungenen die bijvoorbeeld de adaptieve immuunrespons (T- & B-cellen) en de productie van immunoglobulinen reguleren, waren gehypomethyleerd. De auteurs beweerden dat deze bevindingen in lijn lagen met de gerapporteerde verbeteringen door Rituximab.
Promotors (MMP14, MAP4K4, MAPK12 en CREB5), die mogelijk de signalerende reactiepaden van de tumornecrosefactor activeren en zo bijdragen aan de ontstekingsproblemen die bij ME/CVS aanwezig zijn, waren ook gehypomethyleerd.
Een gen (miRNA-148a) dat de aangeboren immuunrespons aantast, was ook gehypomethyleerd. Een aantal van de gehypomethyleerde genen werden reeds gevonden in eerdere ME/CVS-onderzoeken.
Dan is er nog het IL21-gen. De hypomethylatie van de IL21R-genpromotor in ME/CVS kan ontsteking, auto-immuniteit, schildklieraandoeningen en intestinale ontsteking in gang zetten. IL-21 speelt ook een cruciale rol bij het uitlokken van experimentele auto-immuunencefalomyelitis – een diermodel voor hersenontsteking.
Conclusie
Epigenetica is een relatief nieuwe wetenschap die al heel snel een zegen gebleken is bij de studie van auto-immuniteit en kanker. Er zullen grotere studies moeten komen in ME/CVS, alvorens epigenetica haar potentieel kan bereiken. Maar de studie van de groep van Dr. Klimas gaf al aan dat, net als bij sommige auto-immuunziekten, een toegenomen hypomethylatie mogelijk de expressie van genen verhoogt die ontsteking en auto-immuniteit in ME/CVS stimuleren.
Het meest bemoedigende aspect van epigenetica is de mogelijkheid om de epigenetische veranderingen om te keren die veroorzaakt werd door een pathogeen, toxine of geneesmiddel. Veel meer studie is nodig om epigenitische schuldigen in ME/CVS te isoleren, maar medicatie die de epigenetica beïnvloedt, wordt momenteel al ontwikkeld voor andere ziekten. Eén intrigerend medicijn poogt om de epigenetische veranderingen die door het herpes-simplexvirus worden veroorzaakt, terug te draaien en zo het immuunsysteem te normaliseren. Een andere doorbraak suggereert dat epigenetische veranderingen mogelijk een drijvende factor zijn bij multiple sclerose.
Dit is dus duidelijk een vakgebied om in de gaten te houden.
© Simmaron Research. Vertaling MT, redactie Zuiderzon en Abby, ME-gids.
Identification of Myalgic Encephalomyelitis/Chronic Fatigue Syndrome-associated DNA methylation patterns
Malav S. Trivedi, Elisa Oltra, Leonor Sarria, Natasha Rose, Vladimir Beljanski, Mary Ann Fletcher, Nancy G. Klimas, Lubov Nathanson
Published: July 23, 2018 https://doi.org/10.1371/journal.pone.0201066
Abstract
Background
Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS) is a complex condition involving multiple organ systems and characterized by persistent/relapsing debilitating fatigue, immune dysfunction, neurological problems, and other symptoms not curable for at least 6 months. Disruption of DNA methylation patterns has been tied to various immune and neurological diseases; however, its status in ME/CFS remains uncertain. Our study aimed at identifying changes in the DNA methylation patterns that associate with ME/CFS.
Methods
We extracted genomic DNA from peripheral blood mononuclear cells from 13 ME/CFS study subjects [Fukuda and Canadian case definitions, n.v.d.r.] and 12 healthy controls and measured global DNA methylation by ELISA-like method and site-specific methylation status using Illumina MethylationEPIC microarrays. Pyrosequencing validation included 33 ME/CFS cases and 31 controls from two geographically distant cohorts.
Results
Global DNA methylation levels of ME/CFS cases were similar to those of controls. However, microarray-based approach allowed detection of 17,296 differentially methylated CpG sites in 6,368 genes across regulatory elements and within coding regions of genes. Analysis of DNA methylation in promoter regions revealed 307 differentially methylated promoters. Ingenuity pathway analysis indicated that genes associated with differentially methylated promoters participated in at least 15 different pathways mostly related to cell signaling with a strong immune component.
Conclusions
This is the first study that has explored genome-wide epigenetic changes associated with ME/CFS using the advanced Illumina MethylationEPIC microarrays covering about 850,000 CpG sites in two geographically distant cohorts of ME/CFS cases and matched controls. Our results are aligned with previous studies that indicate a dysregulation of the immune system in ME/CFS. They also suggest a potential role of epigenetic de-regulation in the pathobiology of ME/CFS. We propose screening of larger cohorts of ME/CFS cases to determine the external validity of these epigenetic changes in order to implement them as possible diagnostic markers in clinical setting.
© Trivedi et al., 2018
Citeren?
Trivedi MS, Oltra E, Sarria L, Rose N, Beljanski V, Fletcher MA, et al. (2018) Identification of Myalgic Encephalomyelitis/Chronic Fatigue Syndrome-associated DNA methylation patterns. PLoS ONE 13(7): e0201066. https://doi.org/10.1371/journal.pone.0201066
Identification of Myalgic Encephalomyelitis/Chronic Fatigue Syndrome-associated DNA methylation patterns
Background Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS) is a complex condition involving multiple organ systems and characterized by persistent/relapsing debilitating fatigue, immune dysfunction, neurological problems, and other symptoms not curable for at least 6 months. Disruption of DNA methylation patterns has been tied to various immune and neurological diseases; however, its status in ME/CFS remains uncertain.







