Extracellulaire blaasjes (EV’s) zijn een relatief nieuwe verschijning in het veld van het chronischevermoeidheidssyndroom (ME/cvs). Ze doken voor het eerst op in 2018 en sindsdien hebben ten minste 8 studies ze onderzocht bij ME/cvs. De door de NIH gefinancierde groep rond Ludovic Giloteaux/Maureen Hanson heeft het voortouw genomen met 4 studies.

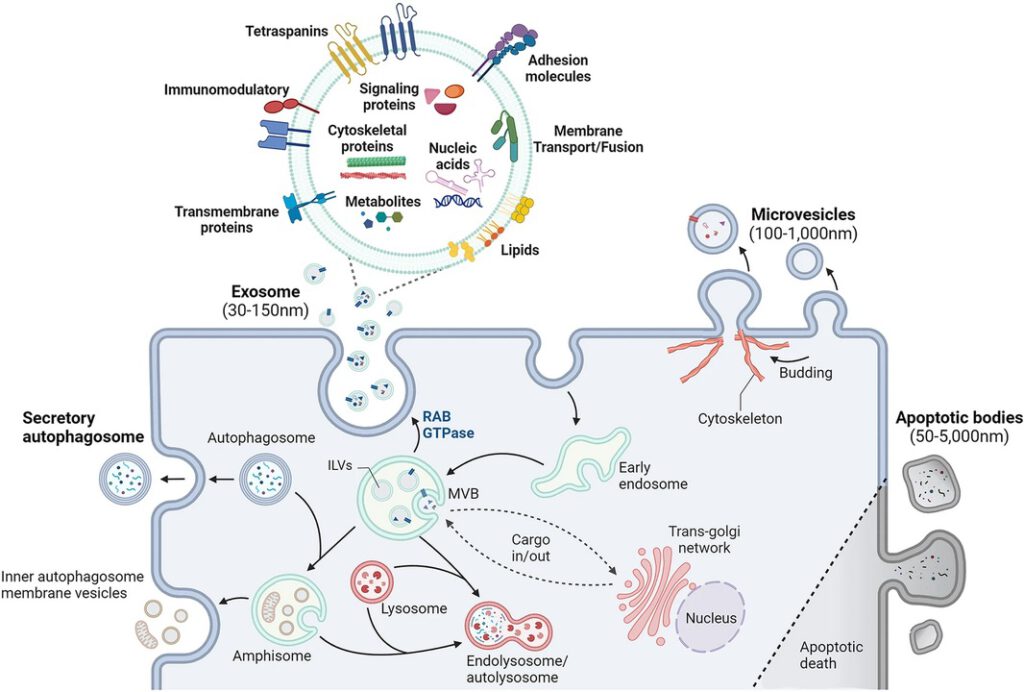
Extracellulaire blaasjes, die in grootte variëren van 30 tot 1.000 nanometer, zijn minuscuul kleine pakketjes (een mensenhaar is 80.000 tot 100.000 nanometer breed) die op regelmatige basis door onze cellen worden uitgestoten. Ze zijn zo klein dat de ontwikkeling van elektronenmicroscopen en ultracentrifuges nodig was om ze te vinden, maar toen ze eenmaal gevonden waren, bleken ze overal te zijn en ze hebben heel wat in hun mars.
Onze cellen communiceren met de rest van het lichaam door EV’s uit te stoten die gevuld zijn met eiwitten, aminozuren, lipiden, DNA en RNA. Ze kunnen veel processen in het lichaam beïnvloeden, waaronder het immuunsysteem en de stofwisseling. Omdat hun samenstelling weerspiegelt wat er op dat moment gebeurt, meten studies hun proteïnegehalte (proteomica), genexpressie (transcriptomica) enz. om een momentopname te krijgen van hoe het lichaam reageert.
In “Dysregulation of extracellular vesicle protein cargo in female myalgic encephalomyelitis/chronic fatigue syndrome cases and sedentary controls in response to maximal exercise”, [“Ontregeling van extracellulaire eiwitvracht bij vrouwelijke gevallen van myalgische encefalomyelitis/chronischevermoeidheidssyndroom en sedentaire controles in respons op maximale inspanning”] onderzocht Giloteaux, in de groep van Maureen Hanson, hoe lichaamsbeweging deze vreemde communicatiemiddelen beïnvloedt bij ME/cvs.
Hun hypothese was dat door het bestuderen van EV’s die vrijkomen tijdens/na inspanning, meer bekend zou worden over wat er gebeurt tijdens inspanning en wat mogelijk de oorzaak is van de malaise na inspanning die mensen met ME/cvs ervaren.
De studie
Aan het door de NIH gefinancierde onderzoek namen 18 vrouwen met ME/cvs deel en 17 leeftijds- en BMI-gematchte sedentaire controles. Bloedmonsters werden verzameld vlak vóór een inspanningstest tot uitputting, en vervolgens 15 minuten en 24 uur later. We hebben gezien dat lichaamsbeweging alles beïnvloedt, van genexpressie tot eiwitten en lipiden op moleculair niveau. Zou dat ook effect hebben op de EV’s?
Het uitblijven van een respons
Dat was het geval. Giloteaux et al. ontdekten dat de EV’s van ME/cvs-patiënten “sterk ontregeld” waren – en op een bekende manier – in vergelijking met de sedentaire maar gezonde controles (HC’s). De studie vond:
- Minder eiwitten in EV’s 15 min na inspanning bij patiënten in vergelijking met controles (Figuur 4a).
- Verminderde eiwitexpressie in EV’s na inspanning bij ME/cvs-patiënten (63 verhoogde EV-eiwitten bij ME/cvs vs. 178 E bij HC’s).
- Uitgestelde respons – een vertraagde toename in de hoeveelheid van verschillende EV-eiwitten na inspanning.
De auteurs concludeerden dat de ME/cvs-patiënten “op moleculair niveau een tekortschietende respons op lichaamsbeweging” vertoonden. Het was een bekend thema. In zijn studies naar lichaamsbeweging heeft de groep van Hanson hetzelfde patroon gevonden met betrekking tot eiwitten, metabolieten en genexpressie bij ME/cvs-patiënten: om de een of andere reden zijn hun systemen op moleculair niveau gewoon niet in staat om te reageren op lichaamsbeweging.
Het kan ook zijn dat hun systemen reageren op een manier die schadelijk is, maar het algemene idee is dat op het meest basale niveau – het moleculaire niveau – de lichamen van ME/cvs-patiënten er gewoon nauwelijks op reageren. Het is alsof ze als het ware negeren dat het überhaupt gebeurt. Als je bedenkt hoe stressvol lichaamsbeweging is, zou dat veel kunnen verklaren. Je kunt je afvragen in hoeverre problemen met de energieproductie op systemisch niveau hierbij een rol kunnen spelen.
Bekijk enkele verslagen van eerdere blogs over de bevindingen van Hansons team.
- Genexpressie – “Terwijl bij de immuuncellen van HC er 102 genen in actie kwamen, hielden de genen in de immuuncellen van de ME/cvs-patiënten zich gedeisd. Ze lieten de inspanning eigenlijk voor wat het was – er werden geen significante veranderingen in genexpressie gevonden.”
- Metabolieten – “Een klein onderzoek naar metabolomica in de urine vond een exploderende hoeveelheid veranderde metabolieten (n=400) bij gezonde controles, maar geen significante verandering in de metabolieten van ME/cvs-patiënten 24 uur na de inspanning.”
- Eiwitten – ” De studie van Germain ontdekte dat lichaamsbeweging een veel grotere verandering teweegbracht in de eiwitten van de sedentaire, maar gezonde controles dan bij de ME/cvs-patiënten. De gezonde controles reageerden op de beproevingen van de tweede inspanningstest door hun proteïnenmix nog meer te herschikken. De ME/cvs-patiënten hadden dat vermogen niet.”
En nu kunnen we EV aan de reeks toevoegen. Als ze dieper in het onderzoek doken, ontdekten de onderzoekers het volgende:
- Meer EV’s bij ME/cvs – Ondanks het feit dat de EV’s bij ME/cvs-patiënten niet zo uitgebreid reageerden op lichaamsbeweging, stootten de cellen van ME/cvs-patiënten ze blijkbaar vaker af, aangezien er over het geheel genomen meer EV’s werden gevonden. De auteurs legden niet uit waarom dit zo zou zijn, maar merkten wel op dat hogere concentraties EV’s zijn gevonden bij andere aandoeningen, waaronder de ziekte van Alzheimer en vasculaire aandoeningen die de hersenen aantasten.
De krankzinnige coagulatiecascade
Door te kijken naar de routepaden die wel of niet geactiveerd werden bij de EV’s, ontdekten de onderzoekers dat lichaamsbeweging een toename in stollingsactiviteit teweegbracht bij zowel ME/cvs-patiënten als bij de gezonde controles, maar ook dat de gevonden stollingsroutes anders waren bij de mensen met ME/cvs.
Verschillende stollingscascade-eiwitten (factoren VIII en XIII AI, fibronectine) waren 15 minuten later significant verlaagd bij ME/cvs. Op dezelfde manier waren verschillende stollingsfactoren die geassocieerd zijn met inspanning bij gezonde mensen (FN1, FGA, FGG of FGB) niet verhoogd na inspanning bij ME/cvs-patiënten. Bij een ziekte die gekenmerkt wordt door verhoogde niveaus van microstolling, leek de afname in sommige delen van de stollingscascade verrassend.
Aan de andere kant waren factoren geassocieerd met fibrinogeen (FGA, FGB en FGG), dat de eigenlijke stolsels vormt, positief gecorreleerd met verhoogde vermoeidheid en PEM na inspanning bij ME/cvs. Ook eiwitten die betrokken zijn bij bloedplaatjes (‘degranulatie’ en ‘aggregatie’ van bloedplaatjes) en wondgenezing waren sterk gecorreleerd met de spierpijn bij ME/cvs.
Op dezelfde manier waren verhoogde plasminogeenspiegels – een nieuwe factor die veel interesse wekte in een recent ME/cvs-onderzoek – “sterk gecorreleerd” met het percentage tijd dat achterovergeleund of neerliggend werd doorgebracht, wat zelf natuurlijk geassocieerd is met hoe ernstig de ME/cvs is. De auteurs stelden dat de verhoogde plasminogeenniveaus een toename weerspiegelden in de stollingsactiviteit of fibrinolyse. De auteurs stelden:
“De veranderde tijdelijke profielen van stollingscascadefactoren in de EV’s van ME/cvs na inspanning onthullen een verstoring in de hemostatische balans tussen stolselvorming en fibrinolyse.”
Lees ook: De mogelijkheden van plasmalogenen voor ME/cvs en langdurige COVID
Dat suggereerde, als ik het goed lees – dat de vorming van stolsels tijdens het sporten wordt geremd bij ME/cvs (!) – precies het tegenovergestelde van wat we zouden verwachten. Aan de andere kant zou het een weerspiegeling kunnen zijn van de pogingen van het lichaam om grote aantallen, moeilijk af te breken stolsels te bestrijden. Wat er ook aan de hand is, de studie suggereerde, net als andere, dat bloedstolling en coagulatie van slag zijn bij ME/cvs. Inderdaad, de auteurs schreven:
“Andere recente rapporten onderbouwen het belang van stollingsprocessen bij ME/cvs” – ze merkten op dat eerdere onderzoeken een 10-voudige toename van microklonters bij ME/cvs hebben gevonden.
Stolling, met al zijn factoren, is een zeer complex proces. De tijd zal leren hoe EV’s de stolling beïnvloeden bij ME/cvs, maar deze studie suggereert dat er iets mis is gegaan met dat proces bij ME/cvs en dat EV’s daar een rol in spelen.
De spieren
Spiercontractie is zo’n beetje het neusje van de zalm als het om lichaamsbeweging gaat. Omdat spieren kracht genereren door samen te trekken, heeft alles wat het vermogen van de spieren om samen te trekken verstoort, invloed op iemands vermogen om te trainen. Het is misschien geen verrassing dat uit een analyse van de routes bleek dat EV’s die betrokken zijn bij spiercontractie, in de top tien stonden van meest veranderde routepaden kort na het sporten bij mensen met ME/cvs.
De myosine light chain-factoren helpen de spieren samentrekken en helpen spierschade te herstellen na het sporten. Van alle eiwitten die werden gevonden in de EV’s van de gezonde controles, vertoonden deze de grootste toename na inspanning. Myosine light chain-factoren (MYL9/MYL12A/MYL9/MYL16) bij mensen met ME/cvs gooiden het echter over een andere boeg: ze waren ofwel verminderd ofwel niet toegenomen.
Ook werd er een verrijking van spierweefsel/-eiwitten gevonden na inspanning bij de gezonde controles, maar een dergelijke verrijking werd niet gevonden bij de mensen met ME/cvs. Verhoogde niveaus van tropomyosine (TPM4), tropomoduline (TMOD3) en calmoduline (CALM2) vanaf de uitgangswaarden tot 24 uur na de inspanning waren sterk gecorreleerd met hogere niveaus van spierpijn bij ME/cvs.
Uiteindelijk werd in de spieren hetzelfde patroon gevonden als in de EV’s in het algemeen – een uitblijven van adequate respons op inspanning. Een verminderde of vertraagde spierrespons van EV’s werd in verband gebracht met meer symptomen bij ME/cvs. Hoewel de auteurs het niet zeiden, zouden vertraagde spierherstelprocessen kunnen resulteren in meer spierschade/pijn na inspanning; m.a.w. PEM.
Merk op dat Rob Wüst in zijn spierbiopsiestudie bij langdurige COVID ontdekte dat lichaamsbeweging vergelijkbare resultaten opleverde, waaronder vaak beschadigd en zelfs afstervend spierweefsel (bij sommige patiënten), en een verhoogde nadruk op het vuile en inefficiënte anaerobe energieproductiesysteem. Wüst is momenteel bezig met een vergelijkbaar onderzoek bij ME/cvs.
Lees ook: Inspanning veroorzaakt spierschade en energie-uitputting bij langdurige COVID
Opstapeling van afval? De clusterine-factor
Een eiwit genaamd clusterine (CLU) sprong er echt uit voor de onderzoekers. Het was de enige factor waar ze een heel deel van het artikel aan wijdden. Clusterine zou een centrale rol kunnen spelen in de vermoeidheid/pijnproblemen die optreden bij ME/cvs. Het was het enige eiwit dat zowel positief gecorreleerd was met de mate van vermoeidheid vóór de inspanning als met de hoeveelheid spier- en gewrichtspijn na de inspanning. Het nam ook in aantal af na inspanning bij de gezonde controles, maar niet bij personen met ME/cvs.
Clusterine is betrokken bij een hele reeks opruimprocessen die volgens andere studies mogelijk een rol spelen bij ME/cvs. Het ruimt cellulair afval op, helpt bij het verwijderen van oude en beschadigde cellen en helpt bij het correct vouwen van eiwitten. Kortom, iets als clusterine lijkt logisch te zijn bij een ziekte waarbij ongebruikelijk gevormde amyloïde eiwitten (in de hersenen en stolsels) aanwezig kunnen zijn, en problemen met autofagie (mitochondriale opruiming) kunnen optreden. Omdat intensieve training altijd kleine beschadigingen in de spieren veroorzaakt, spelen opruimprocessen waarschijnlijk een belangrijke rol in de periode na de training.
Bovendien zijn verhoogde CLU-niveaus aangetoond bij verschillende neurodegeneratieve en ontstekingsziekten (inflammatoire myopathie, reumatoïde artritis) en zijn ze in verband gebracht met cognitieve problemen. Het was geen wonder dat de auteurs rapporteerden:
“In onze studie wordt een verhoogde CLU in EV’s na inspanning geassocieerd met ergere spierpijn, gewrichtspijn en vermoeidheid, wat erop wijst dat dit eiwit een belangrijke rol kan spelen in de pathofysiologie van ME/cvs.”
Immuunproblemen
De stress van lichaamsbeweging zou herpesvirussen of andere ziekteverwekkers kunnen reactiveren die de neiging hebben om te reactiveren tijdens stress. Daartoe vonden de onderzoekers bewijs van opwaarts gereguleerde immuunroutepaden die reageren op “antigenpresentatie”; d.w.z. de aanwezigheid van een ziekteverwekker of een andere stof die het immuunsysteem stimuleert.
Conclusie
De Hanson-groep heeft het weer voor elkaar: voor ten minste de vierde keer hebben ze aangetoond dat personen met ME/cvs op moleculair niveau niet alleen niet normaal reageren op lichaamsbeweging, maar op belangrijke punten zelfs helemaal niet reageren. Of men nu eiwitten, metabolieten, genexpressie of EV’s meet, een normale reactie op inspanning treedt om de een of andere reden niet op tijdens de inspanning of erna.

Hoewel niemand weet wat de oorzaak is, suggereert het feit dat het in verschillende onderzoeken in verschillende onderdelen is aangetoond, dat de groep op het juiste spoor zit.
De EV-studie benadrukte disfuncties in enkele belangrijke factoren die een rol spelen bij inspanning, waaronder stolling, spiercontractie, reiniging of afvalverwijdering en immuunproblemen.
Het is fantastisch om de inspanningsproblemen bij ME/cvs gevalideerd te zien op moleculair niveau. De belangrijke volgende stap zou waarschijnlijk zijn om te proberen begrijpen waarom ME/cvs-systemen niet in staat zijn om normaal te reageren op de stress van inspanning.
Het NIH’s Molecular Transducers of Physical Activity in Humans Program (MoTrPAC; Motor…Pac – snap je? Soort van?) zou wat aanwijzingen kunnen geven. Het MoTrPac-initiatief van 2016 is ontworpen om “de invloed van lichaamsbeweging op biologische moleculen” te volgen, wat de studies van Hanson, als ik me niet vergis, net deden. Twee van de 19 oorspronkelijke subsidies gingen naar twee Stanford-onderzoekers (Michael Snyder, Stephen Montgomery) om alle moleculen die zich tijdens of na inspanning vormen te identificeren en te karakteriseren, en Snyder is betrokken geweest bij onderzoek naar ME/cvs.
De tijd zal het leren, maar de groep van Hanson heeft ons een geweldige start gegeven.
De kernpunten
- Onze cellen communiceren met de rest van het lichaam door onooglijk kleine zakjes proteïnen, aminozuren, lipiden, DNA en RNA uit te stoten, die extracellulaire blaasjes (EV’s) worden genoemd. Deze EV’s kunnen veel processen in het lichaam beïnvloeden, waaronder de regulering van het immuunsysteem en de stofwisseling. Omdat hun samenstelling weerspiegelt wat er op dat moment gebeurt, meten studies hun proteïnegehalte (proteomica), genexpressie (transcriptomica), enz. om een momentopname te krijgen van hoe het lichaam hierop reageert.
- Het was dan ook geen verrassing dat het team van Gilotreaux en Hanson in Cornell ze gebruikten om na te gaan wat er gebeurt als personen met ME/cvs zich wagen aan een korte intense inspanning.
- Ze ontdekten dat de EV’s bij de vrouwelijke ME/cvs-patiënten “sterk ontregeld” waren – en op een vertrouwde manier. Net zoals Hanson heeft aangetoond met eiwitten, genexpressie en metabolieten, lieten de EV’s van de ME/cvs-patiënten het gewoon afweten. Dat wil zeggen, bij ME/cvs reageerden veel minder EV’s op de inspanning dan bij de gezonde controles, en als ze reageerden, duurde het vaak langer voordat ze reageerden.
- Deze bevindingen passen in een breed thema dat op het meest basale niveau – het moleculaire niveau – het lichaam van ME/cvs-patiënten er gewoon niet veel op reageert. Het is alsof ze negeren dat het überhaupt gebeurt. Als ze wel reageren, is hun reactie ook vaak verkeerd – wat suggereert dat ze op een schadelijke manier reageren.
- Pathway-analyses gaven aan dat de stollingsroutes veranderd waren bij ME/cvs-patiënten, wat logisch was gezien studies aantoonden dat mensen met ME/cvs 10x meer microklonters hebben dan normaal.
- Omdat spieren kracht genereren door samen te trekken, zal alles wat het vermogen van de spieren om samen te trekken verstoort, iemands vermogen om te trainen beïnvloeden. Het is misschien geen verrassing dat uit een analyse van de pathways bleek dat EV’s die betrokken zijn bij spiercontractie in de top tien stonden van meest verstoorde routepaden kort na inspanning bij mensen met ME/cvs.
- Terwijl eiwitten die betrokken zijn bij spiercontractie drastisch toenamen bij de gezonde controles na het sporten, waren ze verminderd of namen ze niet toe bij ME/cvs. Op dezelfde manier namen EV’s geassocieerd met spiergerelateerd weefsel toe bij de gezonde controles, maar niet bij de mensen met ME/cvs.
- Rob Wüsts recent inspanningsonderzoek met spierbiopsie bij langdurige COVID lijkt sommige van deze bevindingen te bevestigen. Wüst vond vaak beschadigd en zelfs afstervend spierweefsel na inspanning (bij sommige patiënten), en een verhoogde nadruk op het vuile en inefficiënte anaerobe energieproductiesysteem.
- Een eiwit genaamd clusterine (CLU) sprong er echt uit voor de onderzoekers. Het was het enige eiwit dat zowel positief gecorreleerd was met de mate van vermoeidheid vóór de inspanning als met de hoeveelheid spier- en gewrichtspijn na de inspanning. Het nam ook in overvloed af na inspanning bij de gezonde controles, maar niet bij mensen met ME/cvs.
- Clusterine is betrokken bij verschillende processen die volgens andere studies mogelijk verstoord zijn bij ME/cvs. Het ruimt cellulair afval op, helpt bij het verwijderen van oude en beschadigde cellen en helpt bij het correct vouwen van eiwitten. Clusterineniveaus werden in verband gebracht met verhoogde spier- en gewrichtspijn en vermoeidheid. De auteurs suggereerden dat “dit eiwit een belangrijke rol kan spelen in de pathofysiologie van ME/cvs”.
- De onderzoekers suggereerden dat er misschien een herpesvirus gereactiveerd was want ze vonden bewijs van opwaarts gereguleerde immuunroutepaden die reageren op “antigenpresentatie”; d.w.z. de verschijning van een ziekteverwekker of andere stof die het immuunsysteem op gang brengt.
- Hoewel niemand weet wat de oorzaak is van het vreemde gebrek aan een moleculaire reactie op lichaamsbeweging, suggereert het feit dat werd aangetoond dat het zich voordoet in een aantal verschillende gebieden (genexpressie, EV’s, eiwitten, metabolieten) in verschillende onderzoeken, dat de groep op het juiste spoor zit.
© Health Rising, 8 juni 2024. Vertaling Els, redactie admin, ME-gids.





