De kernpunten
- De saga rond “transient receptor potential melastatin 3” (beter bekend als TRPM3) in het chronischevermoeidheidssyndroom (ME/cvs) is een voorbeeld van één groep – en slechts één groep – die zich vastbijt in iets bij ME/cvs en eraan knaagt als een hond aan een bot.
- Sinds de publicatie van hun eerste TRPM3-paper in 2016 (toepasselijk getiteld “Novel identification and characterization of Transient receptor potential melastatin 3 ion channels…”), heeft de groep niet minder dan 17 papers gepubliceerd over de mogelijkheid dat verstoringen in de TRPM3 (en andere TRPM-ionkanalen) bijdragen aan ME/cvs.
- De TRPM3-ionenkanalen controleren de toestroom van natrium en calcium in de cellen en spelen een rol in alles van energieproductie, spiercontractie, neurotransmitters, gezonde celmembranen, opwekking van elektrische signalen, vochtbalans, etc., en zijn betrokken bij een grote diversiteit aan ziekten.
- Op zoek naar een antwoord op de problemen met het slecht functioneren van de naturalkillercellen bij ME/cvs, zocht de groep naar manieren waarop calciumsignalering – een sleutelfactor in NK-celcytotoxiciteit – verstoord zou kunnen zijn, en vond dat in een verstoorde TRPM3-functie. Talrijke kleine onderzoeken bevestigden die bevinding bij ME/cvs, maar ook bij het Golfoorlogsyndroom en langdurige COVID. Verschillende studies suggereerden dat de verlichting die sommige mensen met ME/cvs ondervinden van naltrexone in lage dosering, kan liggen in het vermogen van het medicijn om de ionenkanalen weer te openen en de calciumniveaus te herstellen.
- In een recente publicatie “Potential pathophysiological role of the ion channel TRPM3 in myalgic encephalomyelitis/chronic fatigue syndrome (ME/CFS) and the therapeutic effect of low-dose naltrexone” (Potentiële pathofysiologische rol van het ionenkanaal TRPM3 bij myalgische encephalomyelitis / chronischevermoeidheidssyndroom (ME/cvs)), stelden Wirth en Lohn dat de disfunctie van de ionenkanalen die het Griffith-team vond, waarschijnlijk veel verder reikt dan het immuunsysteem.
- Ze toonden aan hoe een verstoring van deze kleine maar alomtegenwoordige ionenkanalen in de dunne zenuwvezels en de hersenen een grote rol zou kunnen spelen. Het is mogelijk dat onderactieve TRPM3-ionenkanalen de bloedvaten in een vaatvernauwende of verkrampte toestand brengen – een sleutelthema in de oorspronkelijke hypothese van Wirth met betrekking tot ME/cvs.
- TRPM3-geïnduceerde zenuwdegeneratie zou kunnen bijdragen aan “stoornissen in de microcirculatie, radiculaire compressie, reactieve zuurstofsoorten en autoantilichamen”.
- In de hersenen zou remming van de feel-good chemische stof GABA kunnen leiden tot verhoogde waakzaamheid en verhoogde activiteit van het sympathische zenuwstelsel (vecht/vlucht). Die wanverhouding qua energie (hoge energievraag/lage energieniveaus) leidt tot cognitieve problemen, hersenmist en overgevoeligheid voor geluid, licht en andere zintuiglijke prikkels.
- Omdat het GABA-systeem ook de spiertonus en -spanning reguleert, stellen ze dat een TRPM3-disfunctie kan bijdragen aan de pathofysiologie van skeletspieren, wat leidt tot spiervermoeidheid en postexertionele malaise (PEM).
- Ze beweren dat “het onderzoek van een TRPM3-disfunctie cruciaal zou kunnen zijn voor een beter begrip van de pathofysiologie van deze aandoeningen”.
- Wirth en Lohn noemen geen mogelijke TRPM3-ondersteunende behandelingen, maar één supplement en enkele medicijnen zijn een mogelijkheid. Pregnenolon (PS) is een supplement dat zowel Dr. Teitelbaum als Dr. Myhill hebben aanbevolen voor mensen met ME/cvs. PS is een voorloper van oestrogeen, progesteron, testosteron en cortisol en wordt een “neurosteroïde” genoemd – een steroïde die in de hersenen wordt geproduceerd en die de prikkelbaarheid van het zenuwstelsel moduleert. Dr. Myhill noemt pregnenolon “de moeder en grootmoeder van alle steroïdhormonen”.
- Dr. Teitelbaum rapporteerde dat hij vaak lage waarden van pregnenolon vindt bij ME/cvs. Hij gelooft dat het een onderliggende infectie kan weerspiegelen en heeft een supplementenschema voorgesteld om dat te bestrijden. (Zie blog). Verwijzend naar de chronische stress die het lichaam van ME/cvs-patiënten ervaart, schreef Dr. Myhill dat “pregnenolon bijzonder relevant kan zijn bij de behandeling van het chronischevermoeidheidssyndroom”. Tijdens chronische stress leidt een “tekort aan pregnenolon” ertoe dat er meer stresshormonen worden geproduceerd ten koste van geslachtshormonen zoals testosteron, oestrogeen en progesteron.
- Dr. Ronald Hoffman van “Intelligent Medicine” meldt dat PS een endocannabinoïde is, verwant aan CBD (cannabidiol), en net als CBD kan helpen bij pijn, stemming en het verbeteren van het geheugen. Gezien de mogelijke effecten op hormonen, raadt hij aan om het onder toezicht van een arts in te nemen en de bloedwaarden van pregnenolon en zijn metabolieten na verloop van tijd te controleren.
- Een TRPM3-verhogend medicijn genaamd nifedipine wordt vooral gebruikt om bloedvaten te ontspannen en meer bloed te laten doorstromen, en om slokdarmkrampen te behandelen. Het lijkt een neef te zijn van nimodipine dat nuttig kan zijn bij ME/cvs.
- De tijd zal leren of Marshall-Gradisnuk, en Wirth en Lohn, gelijk hebben dat disfunctionele TRPM3-ionenkanalen bijdragen aan, of zelfs de oorzaak zijn van, ME/cvs en soortgelijke ziekten. Het bewijs voor TRPM3-disfunctie bij ME/cvs – nogal wat positieve kleine studies – is breed maar oppervlakkig en grotere studies zijn nodig.
- Hoewel de ogen misschien vertroebelen bij de komst van weer een nieuwe hypothese, opent elke hypothese een nieuw venster en een nieuwe manier om naar deze ziekten te kijken. Ik herinner me dat ik ooit dacht dat het veld stagneerde en op zoek was naar nieuwe ideeën. Nu niet meer. Nu meer ogen dan ooit naar deze ziekten kijken, duiken er steeds meer creatieve ideeën op.
De saga rond “transient receptor potential melastatin 3” (beter bekend als TRPM3) bij het chronischevermoeidheidssyndroom (ME/cvs) is echt een dingetje. Het is een voorbeeld van één groep – en slechts één groep – die zich vastbijt op iets bij ME/cvs en eraan knaagt als een hond aan een bot.
We hebben dit soort eenzijdige focus eerder gezien bij John Chia en zijn werk met enterovirussen, de Williams-Arriza groep en hun focus op het EBV-dUTPase-eiwit, en de Barnden-groep en de hersenstam.
In tegenstelling tot bredere gebieden van ME/cvs-onderzoek zoals metabolomica, cytokines en inspanningsfysiologie hebben de bevindingen van deze groep niet zoveel steun gekregen van het ME/cvs-onderzoeksveld. Toch heeft elke groep een aanzienlijke hoeveelheid onderzoek geproduceerd.
Geen enkele groep illustreert dit patroon beter dan Sonja Marshall-Gradisniks werk met TRPM3-ionenkanalen aan de Griffith Universiteit in Australië in de afgelopen 8 jaar. (De Griffith-groep werkt ook aan andere mogelijke factoren bij ME/cvs).
Sinds de publicatie van het eerste TRPM3-artikel in 2016 (toepasselijk getiteld “Novel identification and characterization of Transient receptor potential melastatin 3 ion channels…”), heeft de groep niet minder dan 17 artikelen gepubliceerd over de kans dat verstoringen in de TRPM3- (en andere TRPM-ionkanalen) bijdragen aan ME/cvs.
Terwijl ionenkanalopathieën al in 2000 werden voorgesteld mogelijk een rol te spelen bij ME/cvs, is het geen probleem om te zeggen dat TRPM3-kanalen vóór 2016 op niemands radar stonden.
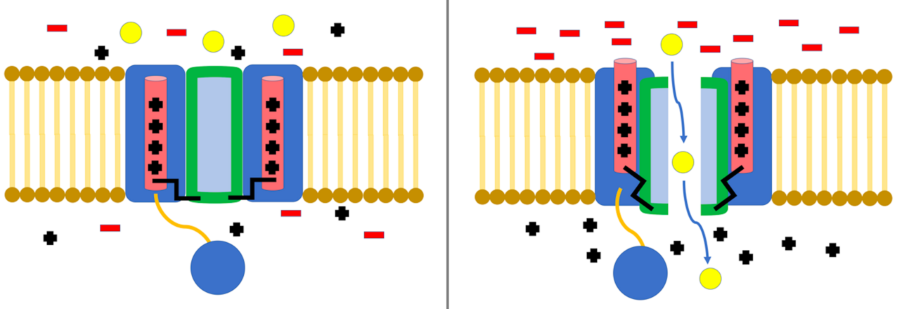
Natrium/Calcium-ionenkanalen in de war?
Ionenkanalen laten ionen zoals natrium, kalium, calcium en chloride door de celmembranen in de cel stromen waar ze allerlei cellulaire functies besturen. De TRPM3-ionenkanalen regelen de toevoer van natrium en calcium in de cellen.
Deze ionen zijn van groot belang. Calcium speelt een rol bij alles van energieproductie, spiersamentrekking, neurotransmitters, genexpressie tot celdood. Natrium helpt de celmembranen gezond te houden en speelt een rol bij het produceren van elektrische signalen, de vochtbalans, het transport van voedingsstoffen en nog veel meer.
Problemen met deze kleine kanaaltjes zijn in verband gebracht met een breed scala aan ziekten, waaronder migraine, epileptische encefalopathieën, chronische pijn, lage rugpijn, werking van bloedvaten, hersenverlamming, oogziekten en nog veel meer. TRPM3-kanalopathieën kunnen zo’n groot bereik hebben omdat ze voorkomen op sensorische neuronen, op gladde spieren in de bloedvaten, in de hersenen en het ruggenmerg, de huid, de alvleesklier, de nieren, de eierstokken, de hypofyse en de teelballen.
Griffiths openingszet voor TRPM3
De TRP-studie van Griffith voor ME/cvs werd gestimuleerd door talrijke bevindingen van NK-celdisfunctie bij ME/cvs. Op zoek naar een antwoord hierop zocht de groep naar manieren waarop calciumsignalering – een sleutelfactor in NK-celcytotoxiciteit – verstoord zou kunnen zijn, en vond dit. Verhoogde niveaus van genetische polymorfismen in TRPM3- (en TRPM8-) ionenkanalen en acetylcholinereceptoren bij ME/cvs suggereerden dat er iets was fout gegaan. Vanaf dat punt was de jacht geopend.
De volgende twee studies vonden verlaagde niveaus van TRPM3-ionenkanalen op naturalkiller- (50% lager) en B-cellen, en een bijbehorende verlaging van intracellulair calcium bij ME/cvs. Omdat het endogene opioïdensysteem en TRPM3-receptoren betrokken zijn bij de pijnproductie, vonden drie laboratoriumstudies een nieuwe verklaring voor de werking van naltrexone in lage doseringen: naltrexone herstelde de activiteit van TRPM3-ionenkanalen bij ME/cvs-patiënten en zorgde voor herstel van de juiste Ca2+-signalering.
Een overexpressie van TRPM2-kanalen op NK-cellen en in TRPM7-ionenkanalen wees op meer mogelijke problemen met calciummobilisering bij ME/cvs. Recente studies vonden ook disfunctionele TRPM3-ionenkanalen bij Golfoorlogsyndroom en langdurige COVID.
Hoewel de meeste Griffith-studies erg klein waren, hebben ze consistent gewezen op TRPM3-ionenkanaaldisfunctie bij ME/cvs en Golfoorlogsyndroom en langdurige COVID.
TRPM3 in het kwadraat?
Met de recente publicatie van “Potential pathophysiological role of the ion channel TRPM3 in myalgic encephalomyelitis/chronic fatigue syndrome (ME/CFS) and the therapeutic effect of low-dose naltrexone” (Potentiële pathofysiologische rol van het ionenkanaal TRPM3 bij myalgische encephalomyelitis / chronischevermoeidheidssyndroom (ME/cvs) en het therapeutische effect van naltrexone in lage dosis), vervoegden Wirth en Lohn, misschien niet verrassend, zich in de TRPM3-strijd.
In 2016 stelden Wirth en Scheibenbogen dat intracellulaire calciumproblemen, veroorzaakt door problemen met een natriumtransporteur, een centrale rol spelen in de energieproductieproblemen bij ME/cvs. Sindsdien heeft Wirth in een reeks hypothesepapers hun oorspronkelijke ideeën sterk uitgebreid. Zie hieronder.
Wirth en Lohn begonnen hun huidige hypothesepaper met een uitgebreide opmerking, waarin ze stelden dat het “onwaarschijnlijk is dat de disfunctie van ionenkanalen (bij ME/cvs) beperkt is tot een enkel orgaan of celtype…”, en ze beweerden: “Een geïsoleerde TRPM3-disfunctie uitsluitend in NK-cellen is geen bevredigende verklaring voor de pathofysiologische rol van TRPM3 bij ME/cvs.”
Ze wezen er ook op hoe verschillend ziekten als ME/cvs kunnen zijn. Terwijl verhoogde TRPM3-activiteit en calciumniveaus in verband zijn gebracht met ME/cvs-achtige symptomen zoals cognitieve en musculoskeletale problemen en pijn – houden de TRPM3-problemen bij ME/cvs een “verlies van functie” in; d.w.z. verminderde TRPM3-activiteit en verlaagde calciumniveaus. Tot ME/cvs opdook, waren er geen ziekten in verband gebracht met een verminderde TRPM3-werking.
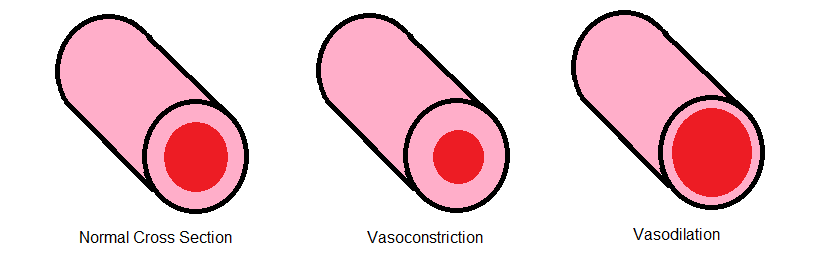
Ze legden uit hoe een verstoring van deze kleine maar alomtegenwoordige ionenkanalen in de dunne zenuwvezels en de hersenen een grote rol zou kunnen spelen bij ME/cvs. Ze geloven dat onderactieve TRPM3-ionenkanalen kunnen resulteren in verlaagde CGRP-niveaus, waardoor de bloedvaten in een vasoconstrictieve, of vernauwde toestand, blijven – een sleutelthema in de oorspronkelijke hypothese. Verminderde CGRP-spiegels resulteren in een natriumoverbelasting, verhoogde intracellulaire calciumspiegels en uiteindelijk in een mitochondriale disfunctie.
Wat de dunne zenuwvezels betreft, schrijven ze, “het is moeilijk te geloven dat een functioneel defect van TRPM3 zoals gevonden bij naturalkillercellen… uiteindelijk niet betrokken zou zijn bij de degeneratie van de dunne zenuwvezels”, en ze stelden vervolgens dat de TRPM3-geïnduceerde zenuwdegeneratie zou kunnen bijdragen aan “microcirculatoire verstoringen, radiculaire compressie, reactieve zuurstofsoorten en autoantilichamen”.
Ze suggereren dat onderactieve TRPM3-kanalen in de hersenen de productie van de feel-good chemische stof GABA kunnen remmen. Omdat GABA de opwekkende neurotransmitter glutamaat remt, zou een verminderde GABA-activiteit kunnen resulteren in de overmatige alertheid en verhoogde activiteit van het sympathische zenuwstelsel (vecht/vlucht) die gevonden wordt bij ME/cvs.
Ze merkten op dat de overprikkeling van de hersenen die waarschijnlijk aanwezig is, een dubbele klap toebrengt doordat het plaatsvindt in een brein dat al geen normale hoeveelheden bloed (d.w.z. energie) meer krijgt. Die energie-mismatch (hoge energievraag/lage energieniveaus) leidt tot cognitieve problemen, hersenmist en overgevoeligheden voor geluid, licht en andere zintuiglijke prikkels.
Omdat het GABA-systeem ook de spiertonus en -spanning reguleert, stellen ze dat een TRPM3-disfunctie kan bijdragen aan de pathofysiologie van de skeletspieren, wat leidt tot spiervermoeidheid en postexertionele malaise (PEM).
Bovendien leidt de verhoogde bloeddruk, hartslag en skeletspierspanning als gevolg van mentale stress tot meer energieverbruik, waardoor een kapot energieproductiesysteem nog meer onder druk komt te staan, er nog meer calciumoverbelasting optreedt en waardoor de bloedtoevoer naar de spieren wordt belemmerd, wat leidt tot schade aan de skeletspieren en mitochondriale disfunctie. Dat is een interessant idee gezien de spierpijn die ik vaak associeer met mentale inspanning.
In het algemeen stellen ze dat “een TRPM3-disfunctie een aanzienlijk pathofysiologisch potentieel heeft, dat bijdraagt aan een slechte doorbloeding, mitochondriale disfunctie en degeneratie van de dunne vezels bij ME/cvs”.
Ze beweren dat “het onderzoeken van een TRPM3-disfunctie cruciaal zou kunnen zijn voor het bevorderen van ons begrip van de pathofysiologie van deze aandoeningen.”
Behandelingen? TRPM3-agonisten (versterkers)
Het artikel gaat niet in op behandelingen, maar er zijn enkele TRPM3-versterkende medicijnen ontwikkeld en een recente review noemde TRPM3 “een nieuwkomer op het gebied van pijnbehandeling?”.
De mogelijkheid van pregnenolon
De bekendste bron – pregnenolonsulfaat (PS) – is een supplement. PS is een voorloper van oestrogeen, progesteron, testosteron en cortisol en wordt een “neurosteroïde” genoemd – een steroïde die in de hersenen wordt geproduceerd en de prikkelbaarheid van het zenuwstelsel moduleert. Dr. Myhill noemt pregnenolon “de moeder en grootmoeder van alle steroïde hormonen”.

Dr. Teitellbaum meldde dat hij vaak extreem lage pregnenolonniveaus aantreft bij personen met ME/cvs, wat volgens hem een teken van infectie is. Hoewel hij verklaarde dat hij vond dat pregnenolon kan helpen, meldde hij dat de inname ervan in combinatie met andere supplementen effectiever kan zijn.
In 2011 raadde hij ME/cvs-patiënten, die geen statines slikken en een laag of laag-normaal pregnenolon of laag cholesterolgehalte hebben, aan om drie maanden lang CoQ10 (200-400 mg per dag), pregnenolon (100-200 mg per dag) en omega visolie toe te voegen. Als je ziekte een griepachtig begin had, raadde hij aan om 3 maanden lang 25 mg zink per dag te nemen, daarna 15 mg per dag en eventueel een paar maanden lang een statine toe te voegen.
Verwijzend naar de chronische stress waaronder het lichaam van ME/cvs-patiënten staat, schreef Dr. Myhill dat “pregnenolon bijzonder relevant kan zijn bij de behandeling van het chronischevermoeidheidssyndroom”. Tijdens chronische stress leidt de “pregnenolon-afname” ertoe dat er meer stresshormonen worden geproduceerd ten koste van geslachtshormonen zoals testosteron, oestrogeen en progesteron. Het toevoegen van meer pregnenolon helpt om de stress- en geslachtshormonen weer in balans te brengen. Myhill gebruikt een Adrenal Stress Profile-test om te bepalen of er sprake is van een tekort aan cortisol, en als dat zo is, gebruikt ze pregnenolon in capsules van 50 mg die ze onder de tong laat oplossen.
Dr. Ronald Hoffman van “Intelligent Medicine” meldt dat PS een endocannabinoïde is, verwant aan CBD (cannabidiol), en net als CBD kan helpen voor pijn, humeur en geheugen. Hij stelt dat PS in de jaren vijftig kortstondig werd gebruikt als ontstekingsremmer, maar dat zijn slechte biologische beschikbaarheid ertoe leidde dat het werd afgevoerd. Bezorgd over de effecten op DHEA en andere hormonen, gebruikte hij het in kleine hoeveelheden bij zijn patiënten totdat twee onderzoeken met 500 mg/dag aantoonden dat het hielp bij lage rugpijn en depressie. Hij schreef dat PS nu wordt onderzocht bij multiple sclerose om neuro-inflammatie te onderdrukken.
Toch raadt hij, gezien de mogelijke effecten op hormonen, aan om het onder toezicht van een arts in te nemen en de bloedwaarden van pregnenolon en zijn metabolieten na verloop van tijd te bepalen. Zijn eindoordeel is:
“Het brede scala aan voordelen van pregnenolon, de relatieve afwezigheid van bijwerkingen, het geruststellende feit dat het een van de meest voorkomende natuurlijke hormonen van het lichaam is, en de algemene beschikbaarheid als een vrij verkrijgbaar supplement rechtvaardigen het onderzoek ervan voor een breed scala aan kwalen waarvoor weinig veilige en doeltreffende opties bestaan”.
Geneesmiddelen
Een TRPM3-verhogend medicijn genaamd nifedipine wordt vooral gebruikt om bloedvaten te ontspannen en meer toevoer van bloed door te laten, en om slokdarmspasmes te behandelen. Het lijkt een neef te zijn van nimodipine dat nuttig kan zijn bij ME/cvs.
Lees ook: Nimodipine For Chronic Fatigue Syndrome (ME/CFS) and Fibromyalgia
Misschien wel de krachtigste TRPM3-versterker – een medicijn genaamd CIM0216 – is alleen beschikbaar voor onderzoeksdoeleinden. Op langere termijn is er het medicijn dat Wirth en zijn bedrijf op de markt proberen te brengen voor de behandeling van ME/cvs.
Lees ook: Onderzoek naar spieren bij ME/cvs resulteert in opstarten van farmaceutisch bedrijf
Conclusie
De tijd zal het leren of Marshall-Gradisnik, en Wirth en Lohn, gelijk hebben dat disfunctionele TRPM3-ionenkanalen bijdragen tot, of zelfs de oorzaak zijn van, ME/cvs en gelijkaardige ziekten. Het bewijs voor een TRPM3-disfunctie bij ME/cvs – nogal wat positieve kleine studies – is breed maar magertjes en er zijn grotere studies nodig. Toch is het goed om te zien dat twee verschillende groepen – de Griffith-groep met zijn focus op immuuncellen, en de Wirth en Lohn-groep met hun focus op het functioneren van bloedvaten en energieproductie – bij elkaar aansluiten.
Hoewel de ogen misschien vertroebelen bij de komst van weer een nieuwe hypothese, opent elke hypothese een nieuw venster en een nieuwe manier om naar deze ziekten te kijken. Ik herinner me dat ik ooit dacht dat het vakgebied stagneerde en op zoek was naar nieuwe ideeën. Nu niet meer. Nu er meer ogen dan ooit naar deze ziekten kijken, duiken er steeds meer creatieve ideeën op.
© Health Rising, 20 augustus 2024. Vertaling Els, redactie admin, ME-gids.





